
Was ist Gaschromatographie (GC)?
Die Gaschromatographie (GC) ist eine bewährte analytische Methode, mit der sich einzelne Bestandteile eines Stoffgemisches identifizieren und quantifizieren lassen. Sie wird vor allem zur Untersuchung von gasförmigen und flüchtigen Substanzen eingesetzt und zählt zu den wichtigsten Trennverfahren in der modernen Analytik.
Anders als bei flüssigkeitsbasierten Verfahren erfolgt die Trennung der Stoffe bei der Gaschromatographie in einer Trennsäule, durch die ein Trägergas strömt. Die Methode ermöglicht eine schnelle, präzise und kosteneffiziente Analyse selbst kleinster Mengen eines Gemischs.
Wie funktioniert die Gaschromatographie?
Bei der Gaschromatographie wird eine Probe in den Injektor eines Gaschromatographen eingebracht und dort verdampft. Das dabei entstehende Gas wird mithilfe eines Trägergases (z. B. Helium oder Wasserstoff) durch eine sogenannte Trennsäule transportiert. Innerhalb dieser Säule interagieren die Stoffe der Probe unterschiedlich stark mit der stationären Phase, die an der Säulenwand haftet.
Diese Wechselwirkungen führen dazu, dass sich die Komponenten der Probe mit unterschiedlicher Geschwindigkeit durch die Säule bewegen. Die Folge: Sie verlassen die Säule zu verschiedenen Zeiten, der sogenannten Retentionszeit, und werden nacheinander von einem Detektor erfasst.
Die Ergebnisse werden als sogenanntes Chromatogramm ausgegeben: eine grafische Darstellung mit Peaks, die jeweils für eine Substanz im Stoffgemisch stehen.
Ein Gaschromatograph sorgt also dafür, dass eine Probe automatisiert, kontrolliert und hochpräzise auf ihre Bestandteile analysiert werden kann, unter Einhaltung definierter Temperatur-, Druck- und Flussratenbedingungen.

Vorteile der Gaschromatographie
Die Gaschromatographie bietet eine Vielzahl von Vorteilen gegenüber anderen analytischen Verfahren. Sie ist besonders geeignet, wenn flüchtige oder leicht verdampfbare Verbindungen in einem Gemisch genau identifiziert und quantifiziert werden sollen.
Das zeichnet die Gaschromatographie aus:
- Hohe Trennschärfe: Auch sehr ähnliche Moleküle lassen sich zuverlässig auftrennen
- Schnelle Analysen: Kurze Laufzeiten ermöglichen hohe Probenzahlen pro Tag
- Hohe Empfindlichkeit: Nachweis auch geringster Stoffkonzentrationen
- Breites Anwendungsspektrum: Von der Lebensmittelkontrolle bis zur Umweltanalytik
- Kopplungsmöglichkeit mit MS: Kombination mit Massenspektrometern (GC-MS) erlaubt noch präzisere Aussagen
- Kosteneffizienz: Geringe Betriebskosten und schneller Durchsatz
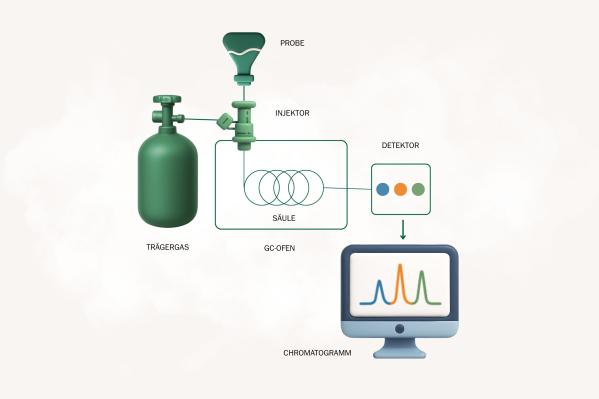
Aufbau eines Gaschromatographen
Injektor: Hier wird die Probe eingebracht und verdampft. Die Verdampfung ist notwendig, damit die Probe in die gasförmige Phase übergeht.
Trägergas-System: Das Trägergas (meist Helium, Wasserstoff oder Stickstoff) transportiert die verdampfte Probe durch das System. Es muss sehr rein sein, um keine Verfälschungen im Ergebnis zu verursachen.
Trennsäule: Das Herzstück des Geräts. Hier findet die eigentliche Auftrennung der Stoffgemische statt. Man unterscheidet zwischen Kapillarsäulen und gepackten Säulen. In der stationären Phase, die die Innenwand der Säule beschichtet, kommt es zu Wechselwirkungen mit den einzelnen Verbindungen.
Temperatursteuerung: Ein Ofen reguliert die Temperatur innerhalb der Trennsäule, da die Trennung vieler Substanzen stark temperaturabhängig ist. Die Methode nennt sich temperaturprogrammierte Gaschromatographie.
Detektor: Am Ende der Säule misst der Detektor die Konzentration der austretenden Analyten. Häufig eingesetzt wird der Flammenionisationsdetektor, aber auch andere Detektortypen sind möglich.
Datenverarbeitung: Die Signale des Detektors werden in einem Chromatogramm grafisch dargestellt und zur weiteren Auswertung gespeichert.
Die Phasen der Gaschromatographie
Die Gaschromatographie trennt Stoffgemische auf Basis der unterschiedlichen Wechselwirkungen der Bestandteile mit zwei Phasen: der mobilen Phase (Trägergas) und der stationären Phase (beschichtete Trennsäule). Wie stark ein Analytenmolekül mit der stationären Phase wechselwirkt, bestimmt seine Retentionszeit; also, wie lange es braucht, um die Säule zu durchlaufen.
Die mobile Phase: das Trägergas
Die mobile Phase ist ein inertes Gas, das die verdampfte Probe durch die Säule transportiert.
Übliche Trägergase sind:
- Helium (He): weit verbreitet, inert, hohe Reproduzierbarkeit
- Wasserstoff (H₂): sehr schnelle Trennung, hohe Effizienz, aber brennbar
- Stickstoff (N₂): günstig, aber geringere Trennleistung bei langen Säulen
Die Wahl des Trägergases beeinflusst Trennzeit, Signalqualität und Detektorkompatibilität.
Die stationäre Phase: das Herz der Trennsäule
Die stationäre Phase ist eine dünne Filmschicht an der Innenwand der Kapillarsäule. Sie besteht meist aus polymeren Materialien, deren chemische Struktur gezielt auf die Eigenschaften der zu trennenden Stoffe abgestimmt ist.
Typische stationäre Phasenmaterialien:
- Polydimethylsiloxan (PDMS): unpolar, Standardphase für viele unpolare Verbindungen
- Poly(ethylene glycol) (PEG): stark polar, ideal für Alkohole, Aldehyde, organische Säuren
- Cyanopropylphenyl-Methylsiloxane: mäßig polar, für ein breites Anwendungsspektrum
- Carbowax®: Handelsname für PEG-basiertes Material
- Wachse und modifizierte Polymere: für spezielle Matrixanforderungen
Die Trennleistung hängt stark von den Eigenschaften der stationären Phase ab, aber ebenso von physikalischen Parametern der Säule.
Einfluss von Länge, Durchmesser und Filmstärke
- Säulenlänge: Längere Trennsäulen (bis 60 m) ermöglichen höhere Auflösung, aber längere Analysezeiten
- Innendurchmesser (ID): Kleinere Durchmesser (z. B. 0,25 mm) führen zu schärferen Peaks, erfordern aber exakt abgestimmte Flussraten
- Filmdicke: Dickere Filmschichten verlangsamen die Trennung (längere Retentionszeit), erhöhen aber die Beladbarkeit und verbessern die Peakform bei polaren Analyten
Jedes Stoffgemisch benötigt für eine optimale Trennung eine passende Kombination aus Trägergas (mobiler Phase), stationärer Phasenbeschichtung sowie eine Trennsäule, deren Länge, Durchmesser und Filmdicke genau auf die jeweilige Analyse abgestimmt sind. Die Auswahl dieser Parameter ist entscheidend für die Trennschärfe, Signalqualität und letztlich die Aussagekraft des Chromatogramms.
Trennprinzip und Retentionszeit
Das zentrale Ziel der Gaschromatographie ist die möglichst präzise Auftrennung eines Stoffgemisches in seine einzelnen Bestandteile. Grundlage dafür ist die unterschiedliche Verteilung der Analyten zwischen der mobilen (Trägergas) und der stationären Phase (Säulenbeschichtung). Dieser Vorgang wird als Verteilungschromatographie bezeichnet.
Wie funktioniert die Trennung?
Wenn eine Probe in die Trennsäule gelangt, interagieren ihre Komponenten unterschiedlich stark mit der stationären Phase. Substanzen, die stärker mit dieser Phase wechselwirken (z. B. durch Van-der-Waals-Kräfte, Polarität oder Molekülgröße), bewegen sich langsamer durch die Säule als solche mit geringerer Affinität.
Diese unterschiedlichen Verweilzeiten führen dazu, dass die Stoffe die Säule zu unterschiedlichen Zeitpunkten verlassen: der sogenannten Retentionszeit.
Wichtige Einflussfaktoren auf die Retentionszeit:
- Chemische Eigenschaften der Substanz (Polarität, Siedepunkt, Molekülmasse)
- Temperatur der Säule (höhere Temperaturen verkürzen die Retentionszeit)
- Beschaffenheit der stationären Phase
- Flussrate des Trägergases
- Geometrie der Säule (Länge, Durchmesser, Filmdicke)
Je ähnlicher sich zwei Verbindungen sind, desto größer ist die Herausforderung, sie zeitlich voneinander zu trennen. Hier spielen hochselektive stationäre Phasen und exakte Temperaturprogramme eine entscheidende Rolle.
Die Retentionszeit ist das wichtigste Maß für die Identifizierung einer Substanz im Chromatogramm. Eine gute Trennung ist nur möglich, wenn die physikalisch-chemischen Eigenschaften der Analyten, die Charakteristika der stationären Phase und die Bedingungen im Gerät sorgfältig aufeinander abgestimmt sind.
Detektoren in der Gaschromatographie
Ein Detektor ist das Element im Gaschromatographen, das am Ende der Trennsäule misst, wann und in welcher Menge ein Analytenmolekül die Säule verlässt. Die Auswahl des richtigen Detektortyps ist entscheidend für die Empfindlichkeit, Selektivität und Anwendungstauglichkeit einer Analyse.
Wie funktionieren Detektoren?
Ein Detektor registriert physikalische oder chemische Eigenschaften der aus der Säule austretenden Substanzen, z. B. elektrische Leitfähigkeit, Wärmeleitfähigkeit oder Ionisationsverhalten, und wandelt diese in ein elektrisches Signal um. Dieses wird als Peak im Chromatogramm dargestellt.
Die Höhe des Peaks steht in direktem Zusammenhang mit der Konzentration des Analyts, die Retentionszeit mit seiner Identität.
Gängige Detektortypen in der Gaschromatographie
1. Flammenionisationsdetektor (FID):
- Am häufigsten verwendeter Detektor in der GC
- Verbrennt organische Verbindungen in einer Wasserstoffflamme
- Misst die durch Ionisation erzeugten elektrischen Ströme
- Vorteile: Hohe Empfindlichkeit für nahezu alle organischen Substanzen, robust, linearer Messbereich
2. Wärmeleitfähigkeitsdetektor (TCD):
- Misst die Veränderung der Wärmeleitfähigkeit des Trägergases beim Austritt von Analyten
- Universaldetektor: erkennt nahezu alle Stoffe
- Weniger empfindlich als FID, aber zerstörungsfrei
3. Elektroneneinfangdetektor (ECD):
- Besonders empfindlich für halogenierte Verbindungen (z. B. Pestizide, PCB)
- Nutzt den Effekt, dass bestimmte Moleküle freie Elektronen einfangen
- Hochselektiv, z. B. in der Umweltanalytik
4. Massenspektrometer (MS):
- Wird häufig in Kombination mit GC verwendet (GC-MS)
- Identifiziert Moleküle anhand ihrer Molekülmasse und Fragmentierung
- Ermöglicht strukturbezogene Aussagen
5. Weitere Detektoren:
- Stickstoff-Phosphor-Detektor (NPD): speziell für stickstoff- und phosphorhaltige Verbindungen
- Flammenphotometrischer Detektor (FPD): zur Schwefel- und Phosphoranalyse
- Photoionisationsdetektor (PID): für aromatische Kohlenwasserstoffe
Die Wahl des Detektors hängt von den zu analysierenden Substanzen, der benötigten Nachweisgrenze und der Matrix der Probe ab. Für viele Routineanalysen ist der FID erste Wahl. Für spezifische Fragestellungen bieten sich selektive oder strukturaufklärende Detektoren wie der ECD oder das Massenspektrometer an.
Chromatogramm und Peaks verstehen
Das Chromatogramm ist das zentrale Ergebnis einer gaschromatographischen Analyse. Es handelt sich dabei um ein grafisches Diagramm, das den Signalverlauf des Detektors über die Zeit abbildet. Jeder Peak entspricht einem einzelnen Analyten, der zu einem bestimmten Zeitpunkt (Retentionszeit) aus der Trennsäule austritt und vom Detektor erfasst wird.
Aufbau eines Chromatogramms
X-Achse: Die Zeit (meist in Minuten) zeigt die Retentionszeit jedes Analyten
Y-Achse: Die Signalstärke gibt die Konzentration des Stoffes wieder
Peaks: Jede Spitze stellt einen detektierten Stoff dar. Die Fläche unter dem Peak ist proportional zur Stoffmenge.
Was sagt ein Peak aus?
Lage des Peaks: Bestimmt die Identität des Stoffes über die Retentionszeit
Höhe oder Fläche des Peaks: Gibt Aufschluss über die Konzentration bzw. Menge des Stoffes
Form des Peaks: Idealerweise symmetrisch. Asymmetrische Peaks können auf Überladung, Matrixeffekte oder technische Probleme hinweisen
Peak-Formen und ihre Bedeutung
Schmaler, hoher Peak: Gute Trennung, hohe Empfindlichkeit
Breiter Peak: Möglicherweise unzureichende Trennung oder zu langsame Flussrate
Doppelte oder überlappende Peaks: Hinweis auf nicht vollständig getrennte Komponenten
Tailing oder Fronting: Verformte Peaks werden oft durch Wechselwirkungen mit Injektor oder Säule verursacht
Ein korrekt interpretiertes Chromatogramm liefert sowohl qualitative als auch quantitative Informationen zu einem Stoffgemisch. Für präzise Ergebnisse ist nicht nur die Trennung, sondern auch die saubere Darstellung der Peaks entscheidend. Die Signalform, die Retentionszeit und die Peakfläche sind die Schlüsselfaktoren zur Identifikation und Mengenbestimmung der einzelnen Verbindungen.

Anwendungsbereiche in der Analytik
Die Gaschromatographie ist eine bewährte Methode zur Analyse flüchtiger und halbflüchtiger Verbindungen mit breitem Einsatzspektrum in der Lebensmittel-, Umwelt-, Kosmetik- und Pharmabranche.
Qualitative Analysen: Welche Substanzen sind enthalten?
Bei der qualitativen Analyse identifiziert die Gaschromatographie einzelne Verbindungen anhand ihrer Retentionszeit im Chromatogramm. Durch den Vergleich mit Referenzstandards lässt sich bestimmen, welche Stoffe in einer Probe enthalten sind.
Typische Einsatzgebiete:
- Rückstandsanalyse von Pestiziden in Obst und Gemüse
z. B. zur Einhaltung gesetzlicher Rückstandshöchstgehalte in der Lebensmittelanalytik - Nachweis von Lösungsmittelrückständen in Kosmetika
z. B. bei der Prüfung ätherischer Öle oder Parfümbestandteile - Bestimmung von Aromakomponenten in Getränken und Spirituosen
z. B. Authentizitätskontrolle bei Wein- und Getränkeuntersuchungen - Screening auf Umweltkontaminanten in Boden- oder Wasserproben
z. B. Analyse von PAKs, VOCs oder Pestiziden in der Umweltanalytik
Die qualitative GC-Analyse liefert ein präzises Stoffprofil zur Produktsicherheit, Authentizitätsprüfung oder zur Aufdeckung unerwünschter Verunreinigungen.
Quantitative Analysen: Wie viel ist enthalten?
Für die quantitative Analyse misst die GC die Fläche unter den Peaks, die proportional zur Konzentration des jeweiligen Stoffes ist.
Typische Einsatzgebiete:
- Gehaltsbestimmung von Mineralölrückständen (MOSH/MOAH) in Lebensmitteln
z. B. bei Schokolade, Backwaren oder Verpackungseinflüssen - Messung von Restlösemitteln in Nahrungsergänzungsmitteln
z. B. nach Herstellungsprozessen mit Ethanol, Hexan o. ä. - Quantifizierung von Rückständen aus Reinigungsmitteln in Kosmetika
z. B. Detektion von Isopropanol, Aceton oder Limonen - Bestimmung von Restalkohol in „alkoholfreien“ Getränken
zur Einhaltung der 0,5 Vol.-% Grenze
GC-MS-Kopplung: Warum und wann?
In der klassischen Gaschromatographie erfolgt die Identifizierung der Verbindungen über ihre charakteristische Retentionszeit. Doch nicht immer reicht diese Information aus, um einen Stoff eindeutig zu bestimmen, zum Beispiel bei überlappenden Peaks, ähnlichen Molekülstrukturen oder komplexen Matrizes. In solchen Fällen wird die GC mit einem Massenspektrometer kombiniert: ein Verfahren, das als GC-MS bezeichnet wird.
Wie funktioniert GC-MS?
Die GC-MS-Kopplung vereint zwei leistungsstarke Methoden:
- Die Gaschromatographie trennt die Bestandteile der Probe zeitlich auf.
- Die Massenspektrometrie analysiert im Anschluss jedes Molekül einzeln, indem es ionisiert und in charakteristische Fragmentmuster zerlegt wird.
Diese Muster, die Massenspektren, sind eindeutig und dienen als molekulare „Fingerabdrücke“, mit denen sich Substanzen präzise identifizieren lassen.
Vorteile der GC-MS-Kopplung
- Eindeutige Identifikation auch bei sehr ähnlichen Substanzen
- Höchste Empfindlichkeit für Spurenanalytik im niedrigen ppb- oder ppt-Bereich
- Strukturaufklärung unbekannter Substanzen durch charakteristische Fragmentierung
- Zuverlässige Ergebnisse auch bei komplexen Probenmatrizes
GC-MS ist besonders dann hilfreich, wenn keine klaren Referenzwerte für Retentionszeiten existieren oder wenn unerwartete Verbindungen detektiert werden. Auch bei rechtlich regulierten Stoffgruppen, wie Pestiziden oder Umweltkontaminanten, wird GC-MS häufig eingesetzt, um eindeutige Nachweise zu liefern.
Gaschromatographie bei Tentamus: präzise Analytik für Ihre Produkte
Die Gaschromatographie ist ein hochentwickeltes Verfahren, das in der Praxis eine präzise Abstimmung zahlreicher Faktoren erfordert: von der Auswahl geeigneter Trennsäulen und Detektoren bis zur Interpretation komplexer Chromatogramme. Unsere Labore arbeiten mit modernster Gerätetechnik und validierten Methoden, abgestimmt auf Ihre konkrete Fragestellung.
Verlassen Sie sich auf langjährige Erfahrung, persönliche Beratung und die Qualität eines nach DIN EN ISO/IEC 17025 akkreditierten Labornetzwerks.
Unsere Expertenteams unterstützen Sie bei:
- Auswahl geeigneter GC-Methoden für Ihre Probe
- qualitativen und quantitativen Analysen
- Rückstandsanalytik, Identitätsprüfung und Verunreinigungskontrolle
- Validierung und Dokumentation für gesetzliche Anforderungen
Sie möchten mehr über unsere gaschromatographischen Leistungen erfahren oder eine Analyse beauftragen?
FAQ: Häufig gestellte Fragen zur Gaschromatographie
1.Wie lange dauert eine Gaschromatographie?
Je nach Methode dauert eine GC-Analyse wenige Minuten bis etwa eine Stunde. Die genaue Dauer hängt von der Art der Probe, der Säulenlänge und dem Temperaturprogramm ab. Inklusive Probenvorbereitung, Auswertung usw. sind die Ergebnisse nach ein paar Werktagen verfügbar.
2.Was kostet eine Gaschromatographie-Analyse?
Die Kosten variieren je nach Analysetiefe, Probenmatrix und Detektionsmethode.
3.Was ist der Unterschied zwischen GC und HPLC?
GC arbeitet mit verdampften Proben und einem Trägergas, HPLC mit flüssigen Proben und einer Flüssigkeitsphase. GC eignet sich für flüchtige Substanzen, HPLC für nicht-flüchtige und thermolabile Verbindungen.
Lesen Sie hier mehr über die Unterschiede zwischen GC und HPLC.
4.Was ist ein Chromatogramm?
Ein Chromatogramm ist die grafische Darstellung der Detektorsignale über die Zeit. Jeder Peak steht für eine bestimmte Substanz im Stoffgemisch.
5.Was bedeutet Retentionszeit?
Die Retentionszeit ist die Zeitspanne, die ein Stoff vom Einbringen bis zum Austreten aus der Trennsäule benötigt. Sie dient zur Identifikation der Substanz.
6.Was ist der Unterschied zwischen einem internen und einem externen Standard?
Ein interner Standard wird der Probe beigemischt und dient als Referenz im gleichen Lauf. Ein externer Standard wird separat analysiert und dient zum Vergleich mit der Probenmessung.
7.Was versteht man unter Headspace-GC?
Headspace-GC analysiert nur die gasförmigen Anteile über einer Probe, z. B. leicht flüchtige Aromastoffe oder Lösungsmittel. Sie ist besonders matrixschonend.
8.Welche Stoffe lassen sich mit Gaschromatographie nicht analysieren?
Nicht-flüchtige, thermisch instabile oder sehr große Moleküle wie Proteine oder Polymere lassen sich mit GC meist nicht analysieren.
9.Welche Faktoren beeinflussen die Trennleistung in der GC?
Die Trennleistung in der Gaschromatographie wird von mehreren physikalischen und chemischen Faktoren beeinflusst. Eine zentrale Rolle spielt die Wahl der Trennsäule. Insbesondere deren Länge, Innendurchmesser und die Dicke der stationären Phase. Auch die Temperaturführung im Säulenofen durch isotherme oder temperaturprogrammierte Verfahren wirkt sich direkt auf die Qualität der Trennung aus.
Weitere Einflussgrößen sind das Trägergas (Art und Flussrate) sowie die chemischen Eigenschaften der zu trennenden Substanzen, wie Polarität, Siedepunkt und Molekülgröße. Nur wenn all diese Parameter aufeinander abgestimmt sind, lassen sich komplexe Stoffgemische mit hoher Auflösung auftrennen.
10.Wer hat die Gaschromatographie entwickelt?
Die moderne Gaschromatographie wurde 1952 von Anthony T. James und Archer J.P. Martin eingeführt, der dafür später den Nobelpreis erhielt.